Grâce à leurs nombreux avantages, les procédés en continu sont courants et souvent plébiscités, notamment lors des étapes USP (Upstream Processing).
Voyons dans cet article les bénéfices certains qu’ils peuvent apporter également pour les phases DSP (Downstream Processing).
Raison 1 : Augmenter la productivité
La productivité d'un procédé biopharmaceutique, qu'il soit continu ou non, peut être définie comme le nombre de grammes de substance médicamenteuse produite, par unité de temps, à un coût donné.
Le coût associé à cette productivité est dépendant de différentes variables : les coûts en capital de l'équipement utilisé pour produire ce médicament, les coûts des matières premières telles que les résines de chromatographie et les milieux de culture cellulaire et les coûts de main-d'œuvre pour effectuer chaque étape de fabrication.
Augmenter la productivité en réduisant le temps de production
Les procédés traditionnels de fabrication en lots sont réalisés en exécutant une étape à la fois.
Au contraire, dans un procédé continu, les étapes sont effectuées en même temps, permettant ainsi de réduire le temps de fabrication.
Prenons l’exemple d’un procédé composé de 4 étapes de purification.
Si ces 4 étapes, auparavant effectuées de manière séquentielle, sont maintenant effectuées simultanément, en gardant le même coût et la même taille de lot, le procédé se termine alors 4 fois plus rapidement et la productivité est multipliée par 4. Ainsi, au lieu d'un procédé de 4 jours pour exécuter 4 étapes, il devient possible de réaliser toutes les étapes en une seule journée !
Cette réduction du temps est particulièrement intéressante pour les entreprises pour lesquelles les calendriers de fabrication sont complets.
Augmenter la productivité en augmentant le volume de produit
En prenant le même exemple d’un procédé composé de 4 étapes de purification.
Le passage au continu peut permettre, non pas de produire 4 fois plus rapidement, mais 4 fois plus pour une production accrue !
Dans ce scénario, le procédé en continu est réalisé pendant la même durée que pour le procédé en lots standard : 4 fois plus de produit médicamenteux est alors fabriqué.
L’établissement d’un procédé en continu permet ainsi aux fabricants d’augmenter leur productivité selon 3 options possibles, dépendamment de leurs priorités : vitesse, volume, coût ou un hybride des trois. La fabrication continue rend la création de produits pharmaceutiques vitaux plus productive et plus efficace.
Raison 2 : Réduire les coûts de production
Un procédé de purification en continu correctement conçu peut réduire les coûts d'équipements jusqu'à 50% par rapport à un procédé en lots standard. Par quels moyens ?
Réduction des tailles de tubings
Lors d’une purification en continu, toutes les étapes sont exécutées de manière simultanée pendant toute la durée du lot. Chaque étape du procédé peut alors être accomplie sur plusieurs jours, voire semaines, plutôt que sur des heures. Ainsi, pour traiter le même volume de lots sur une durée plus longue, le débit du procédé est réduit.
Si nous reprenons notre exemple précédent, si une étape est exécutée pendant 4 jours au lieu de 24 heures, le débit peut être 4 fois inférieur.
L’application de débits plus faibles permet l’utilisation d’une pompe plus petite et de diamètres de tubings plus petits également. Il devient alors possible d’utiliser des tubings moins coûteux, de s’affranchir d’installation en inox onéreuses et ce à toutes les échelles de fabrication biopharmaceutiques.
Réduction des tailles de cuves
Les économies de coûts d'équipement proviennent également d'une réduction de 10 à 1 000 fois des volumes de cuves intermédiaires par rapport à une fabrication conventionnelle.
En effet, toutes les étapes d'un procédé continu étant effectuées simultanément, il n’est plus nécessaire de conserver l'intégralité du volume du lot dans un réservoir pour passer d'une étape à la suivante. Seule une petite cuve est placée dans le trajet d'écoulement entre les étapes connectées en série, principalement pour fournir une rupture de pression.
Le volume minimum de cette cuve n'est limité que par la capacité de l'automatisation à maintenir la cuve dans une plage qui ne provoque pas son débordement ou sa vidange.
De manière concrète, il a été démontré qu'une cuve de rupture/transition avec un temps de séjour de 10 minutes est suffisante pour toutes les étapes d’une purification en continu hormis celles de chromatographie de liaison et d'élution. Ces dernières ayant des élutions périodiques et des concentrations variables, nécessitent une cuve mélangée pouvant contenir environ 5 volumes d'élution, garantissant une solution homogène, fournie à l'étape suivante.
Des essais avec une cuve de rupture de 200 mL et un récipient d'élution de 5 L ont été réalisés pour un lot avec la purification de 1 kg d'anticorps monoclonaux en 4 jours (traitement de 50 L de culture cellulaire par jour). Ces volumes de cuves sont respectivement 500 x et 20 x inférieurs à ceux d’une fabrication traditionnelle.
Les économies d'équipements permises par un procédé en continu sont plus faciles à réaliser lorsqu'une nouvelle installation doit être construite ou qu'une installation existante nécessite un revamping important.
Les installations existantes, quant à elles, obtiennent des avantages mesurables en termes de rendement de production et d'économies de coûts de consommables.
Raison 3 : Réduire les dépenses en consommables
Les procédés de purification en continu génèrent des économies importantes grâce à la réduction des coûts des consommables – en particulier de la résine.
Illustrons avec l’exemple des résines de protéine A coûteuses.
Utiliser des colonnes plus petites
Les purifications en continu permettent des économies de résine pour les produits qui ne traitent généralement pas suffisamment de lots pour atteindre la durée de vie d’une résine avant expiration. Comme vu précédemment, un procédé continu est souvent conçu pour fonctionner lentement sur plusieurs jours ou semaines plutôt que rapidement sur quelques heures.
Par conséquence, des colonnes plus petites sont utilisées pour un plus grand nombre de cycles par rapport à un traitement en lots.
Par exemple, pour purifier 1 kg de mAb par semaine, il est possible d’utiliser une colonne de 4,4 cm de diamètre au lieu d'une colonne de 20 cm, avec moins de 5% du volume de résine.
Il est alors très intéressant de concevoir un procédé de manière à ce que sa durée se rapproche de la durée de vie de la résine pour garantir son utilisation optimale.
Réaliser des chromatographies multicolonnes
Une autre manière de réaliser des économies de coûts de résine consiste à utiliser un système de chromatographie multicolonnes connectant plusieurs colonnes en série. Avec cette configuration, la 1ère colonne de chromatographie peut être chargée à pleine capacité sans perte de rendement qui serait généralement due à une percée du produit - toute percée se liant alors à la 2ème colonne de la série. Dans ce cas-là, un facteur de sécurité pour la capacité de la résine n'est plus nécessaire. Il devient possible d’utiliser un volume de résine inférieur pour une taille de lot donnée.
Les économies de coûts sur les résines, notamment de protéines A dont les tarifs sont les plus élevés sur le marché, sont un moteur important pour les procédés de purification en continu aussi bien pour les installations existantes que nouvelles.
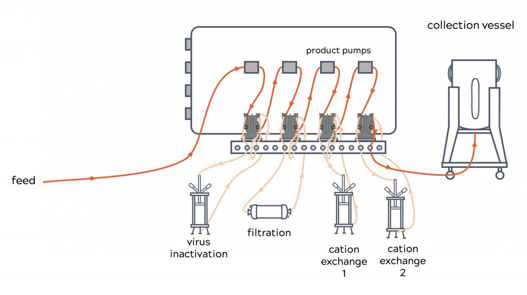 Illustration d'un procédé DSP en continu
Illustration d'un procédé DSP en continu
Les procédés en continu sont aujourd’hui très courants pour les étapes USP. Les nouvelles technologies nous permettent maintenant d’appliquer cette notion aux étapes DSP avec, comme vu dans cet article, des avantages non discutables. Alors n'hésitez pas à nous contacter pour sauter le pas !